 加载中...
加载中...
 日期:2023-08-19
日期:2023-08-19
Xp11.2易位性肾细胞癌(Xp11.2 tRCC)是2016 WHO分型中RCC的一个自力亚群,其特色是转录因子E3 (TFE3)交融基因高表达致使患者预后不良。愈来愈多的研究注解,这些高表达的TFE3交融卵白可以经由过程间接或者直接调控下流靶基因,作为癌症的重要驱动因子。
环状RNA(circRNAs)是一类功效性非编码RNA (ncRNAs),具备由前体mRNA剪接或者跳过事务造成的环状布局,不存于5'结尾帽子以及3'结尾poly(A)尾巴。因为环状布局,环状RNA对于外切酶具备抗性,是以它们的半衰期比线性RNA更长。愈来愈多的证据注解,环状RNA于癌症的发生以及进展中阐扬了主要作用。然而环状RNA与tRCC肿瘤发生相干潜于的份子机制尚不清晰。
近期,南京年夜学医学院李冬梅/甘卫东团队于Molecular Cancer杂志上揭晓题为CircMET promotes tumor proliferation by enhancing CDKN2A mRNA decay and upregulating SMAD3的研究论文,具体论述了circMET于肿瘤中调控细胞增殖的功效及机制。

01 CircMET于NONO-TFE3 tRCC中显著高表达
研究团队经由过程ChIP-seq技能,于NONO-TFE3易位型肾癌(NONO-TFE3 tRCC)中筛选出MET基由于NONO-TFE3的下流靶基因,并评估了circMET于差别RCC细胞系以及一般细胞中的表达程度,发明NONO-TFE3 tRCC患者肿瘤构造的UOK109细胞中表达最高(图1)。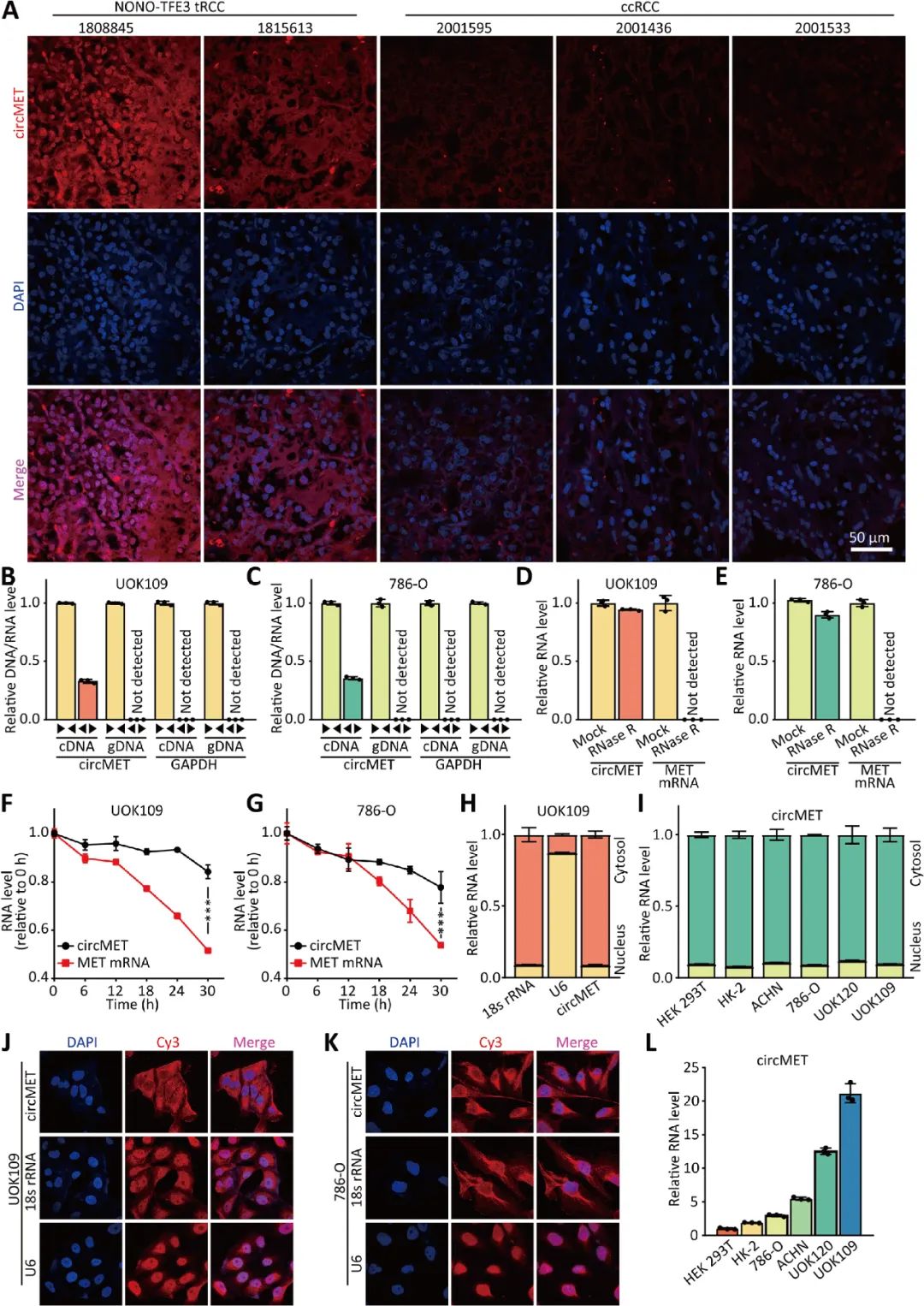 图1 CircMET于NONO-TFE3 tRCC中显著高表达
图1 CircMET于NONO-TFE3 tRCC中显著高表达02 CircMET促成NONO-TFE3 tRCC的增殖
为了确定circMET于NONO-TFE3 tRCC的生物学举动中的功效作用,作者研究了上调或者下调circMET对于癌细胞生长的影响。体外细胞以及体内成瘤试验成果注解circMET促成NONO-TFE3 tRCC的增殖(图2)。
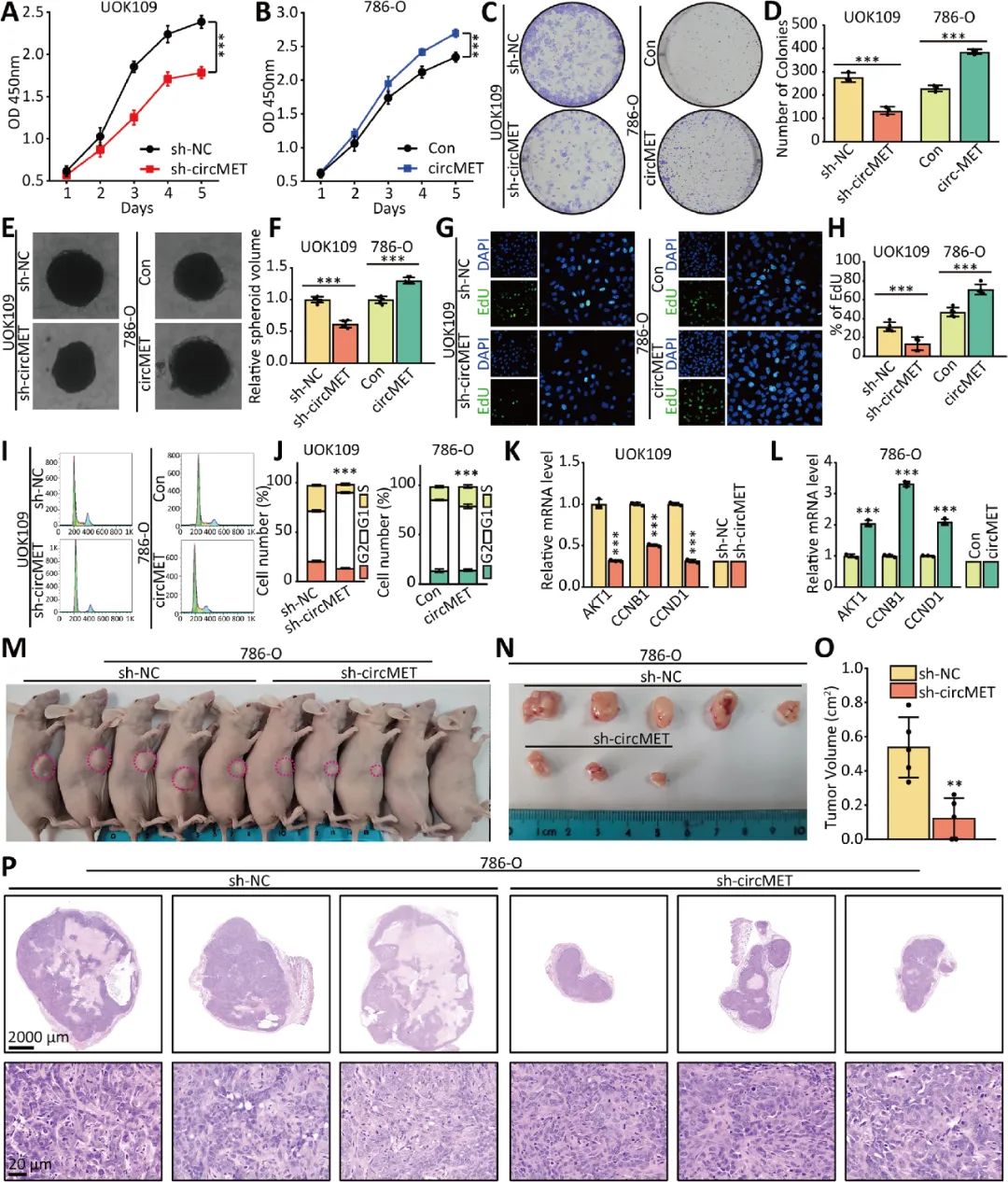 图2 circMET高表达促成NONO-TFE3 tRCC的增殖
图2 circMET高表达促成NONO-TFE3 tRCC的增殖03 NONO-TFE3加强了circMET的转录
研究职员经由过程体外功效缺掉以及功效得到转变NONO-TFE3卵白程度,并别离检测UOK109以及786-O细胞中circMET的表达。双萤光素酶酶试验等注解NONO-TFE3经由过程上调circMET的表达促成NONO-TFE3 tRCC的进展(图3)。
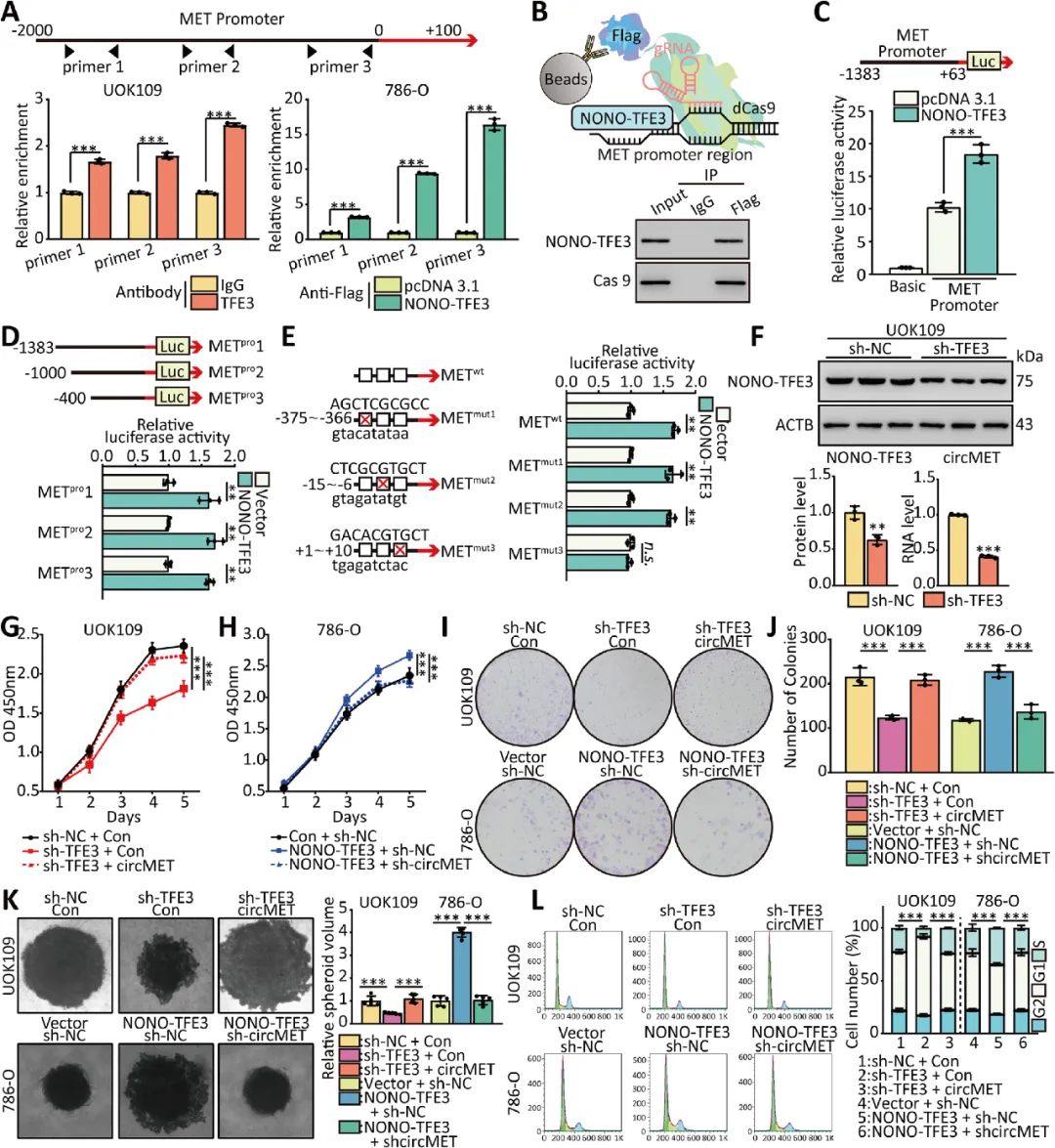 图3 NONO-TFE3加强了circMET的转录
图3 NONO-TFE3加强了circMET的转录04 CircMET经由过程YTHDC1以m6A依靠的体式格局输出到细胞质中
YTHDC1作为m6A解读器卵白的一员,已经知介入RNA剪接以及RNA核输出,研究团队进一步经由过程CRISPR/dCas13构建的靶向去润色体系证明,YTHDC1可经由过程m6A依靠性的体式格局促成circMET出核并阐扬功效(图4)。

05 CircMET经由过程间接联合下调CDKN2A mRNA
circMET已经被证明能促成NONO-TFE3 tRCC的增殖,作者进一步研究circMET是否能调控与细胞周期相干的基因表达,缄默沉静circMET后萤光素酶活性上调最较着的是CDKN2A。CDKN2A是一种肿瘤按捺基因,编码p16卵白,按捺细胞周期。试验证明circMET经由过程间接联合下调CDKN2A mRNA的不变性来促成肿瘤的生长(图5)。
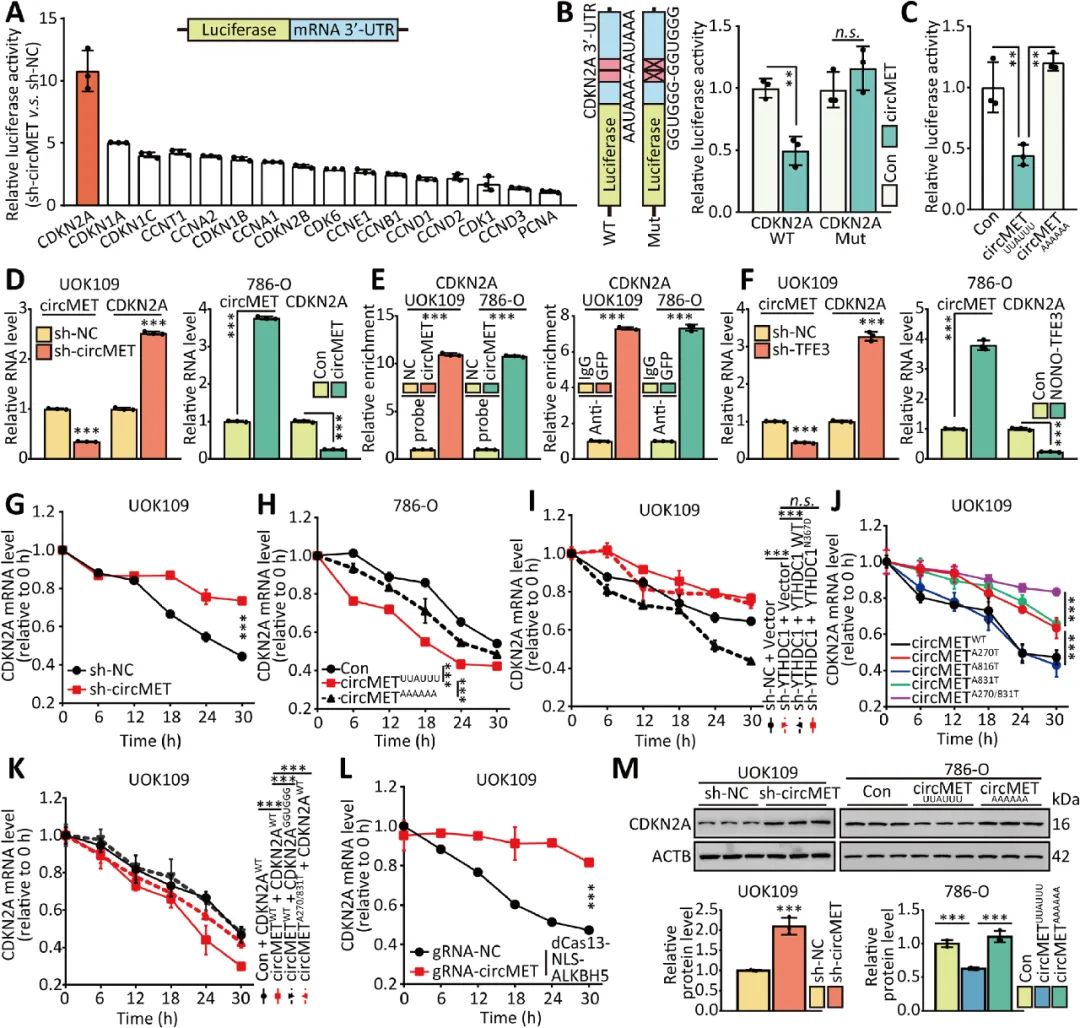 图5 CircMET经由过程间接联合下调CDKN2A mRNA
图5 CircMET经由过程间接联合下调CDKN2A mRNA06 CircMET经由过程招募YTHDF2来加快CDKN2A mRNA的衰减
研究职员进一步证明circMET经由过程与CDKN2A mRNA 3 UTR间接联合,而且召募m6A浏览卵白YTHDF2调控CDKN2A mRNA的降解。circMET召募YTHDF2至CDKN2A mRNA的历程中,YTHDF2间接联合于circMET的m6A润色位点,并介入CDKN2A mRNA的降解历程,而YTHDF2并未间接联合CDKN2A mRNA上的m6A润色位点(图6)。
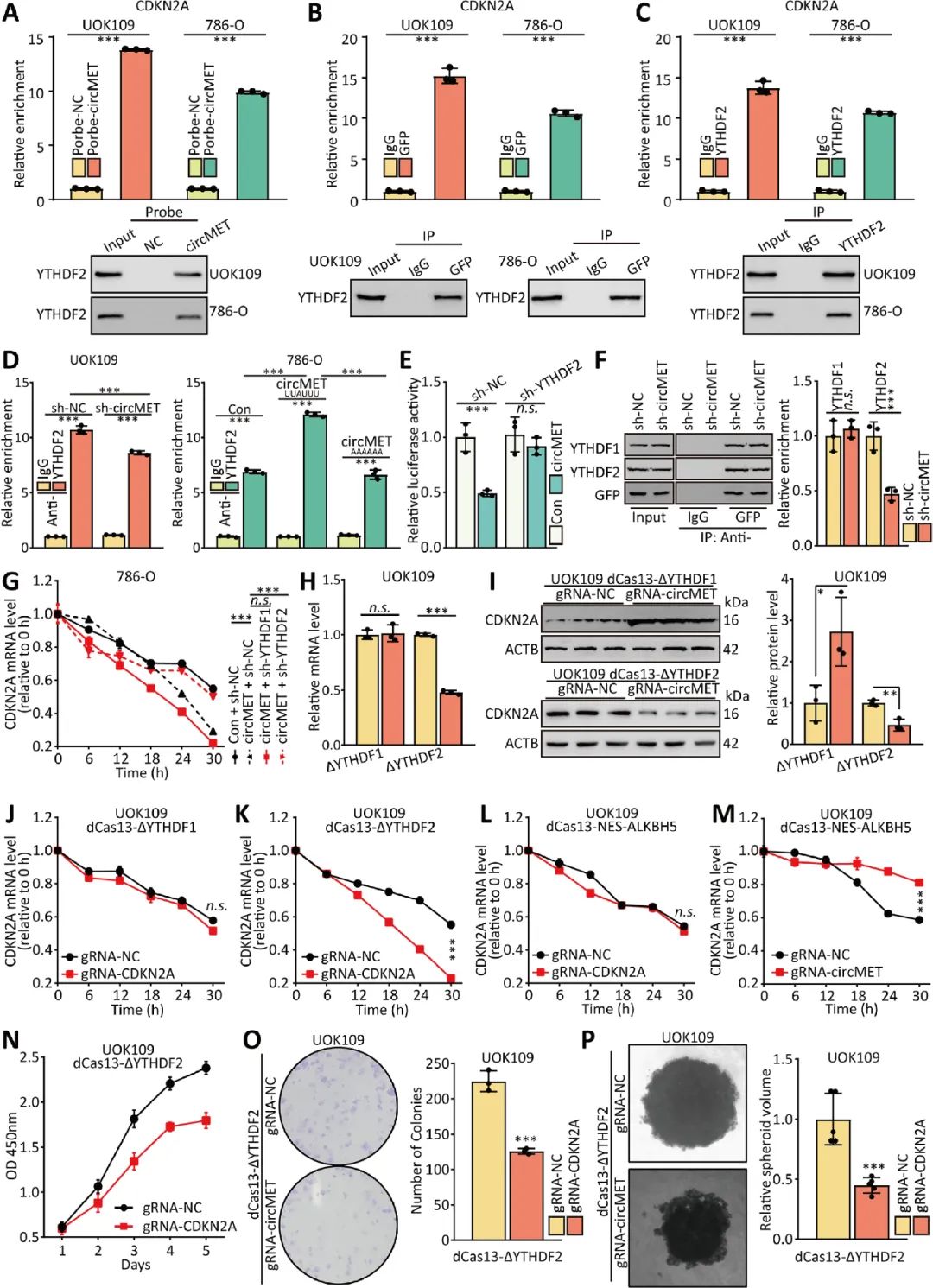 图6 CircMET经由过程招募YTHDF2来加快CDKN2A mRNA的衰减
图6 CircMET经由过程招募YTHDF2来加快CDKN2A mRNA的衰减07 CircMET作为ceRNA来海绵接收miRNAs
年夜量研究证明,环状RNA作为mirRNA的生物海绵,于调控基因表达中阐扬主要作用。circMET于细胞内的漫衍提醒circMET可能也具备转录后调控功效,有助在NONO-TFE3 tRCC的增殖。经由过程软件猜测以及萤光素酶等试验证明miR-1197是circMET潜于的miRNA靶点,细胞程度验证circMET作为ceRNA对于miR-1197具备海绵吸附作用(图7)。
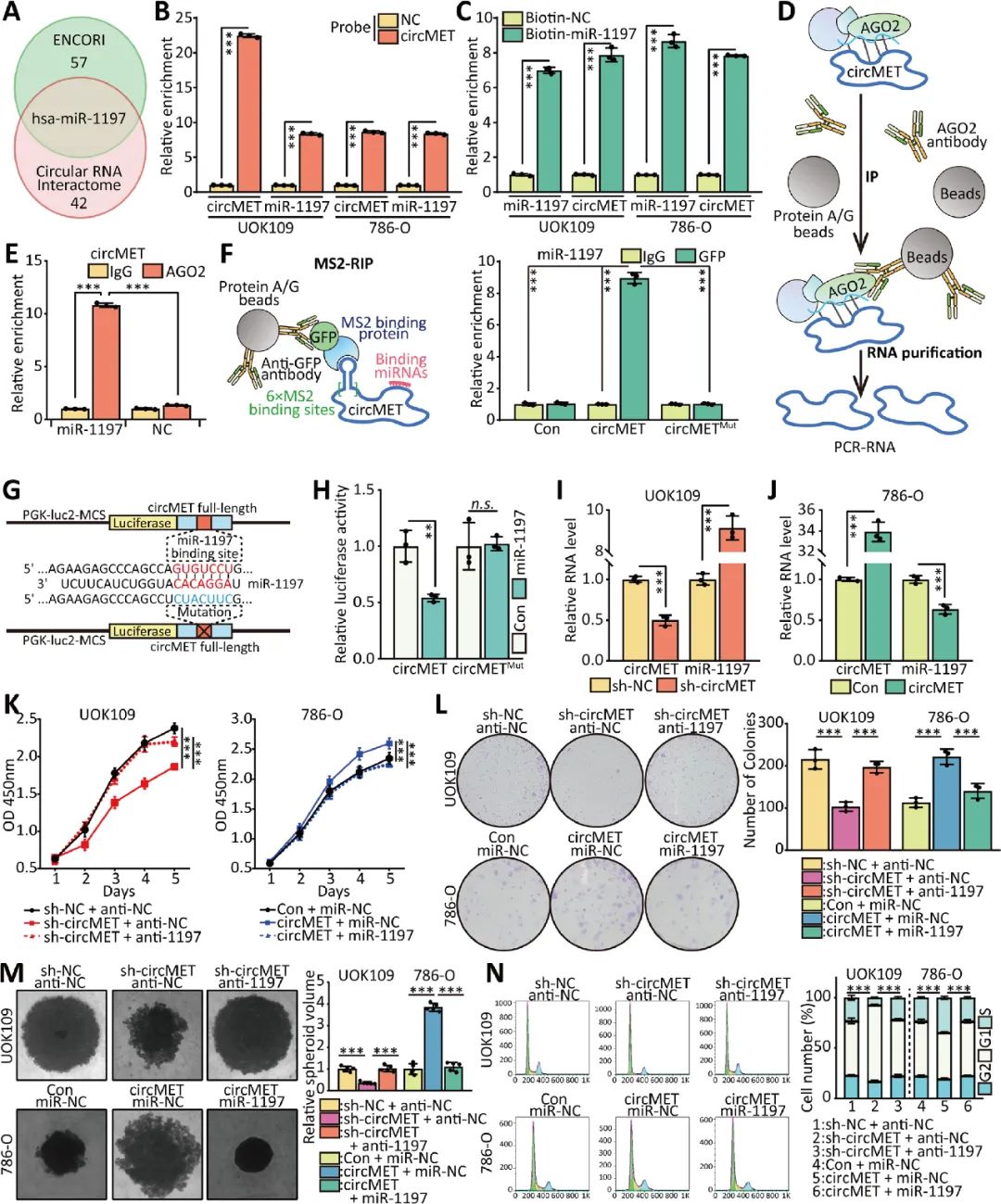 图7 CircMET作为ceRNA来海绵接收miRNAs
图7 CircMET作为ceRNA来海绵接收miRNAs08 CircMET经由过程转录后调控SMAD3的表达
双萤光素酶检测成果显示,过表达miR-1197后,萤光素酶活性下调最较着的是SMAD3, miR-1197可以联合SMAD3 mRNA的3 UTR,并介导NONO-TFE3 tRCC中SMAD3的表达程度。circMET可以经由过程充任miRNAs的 吸附剂 ,经由过程转录后调控SMAD3的表达(图8)。
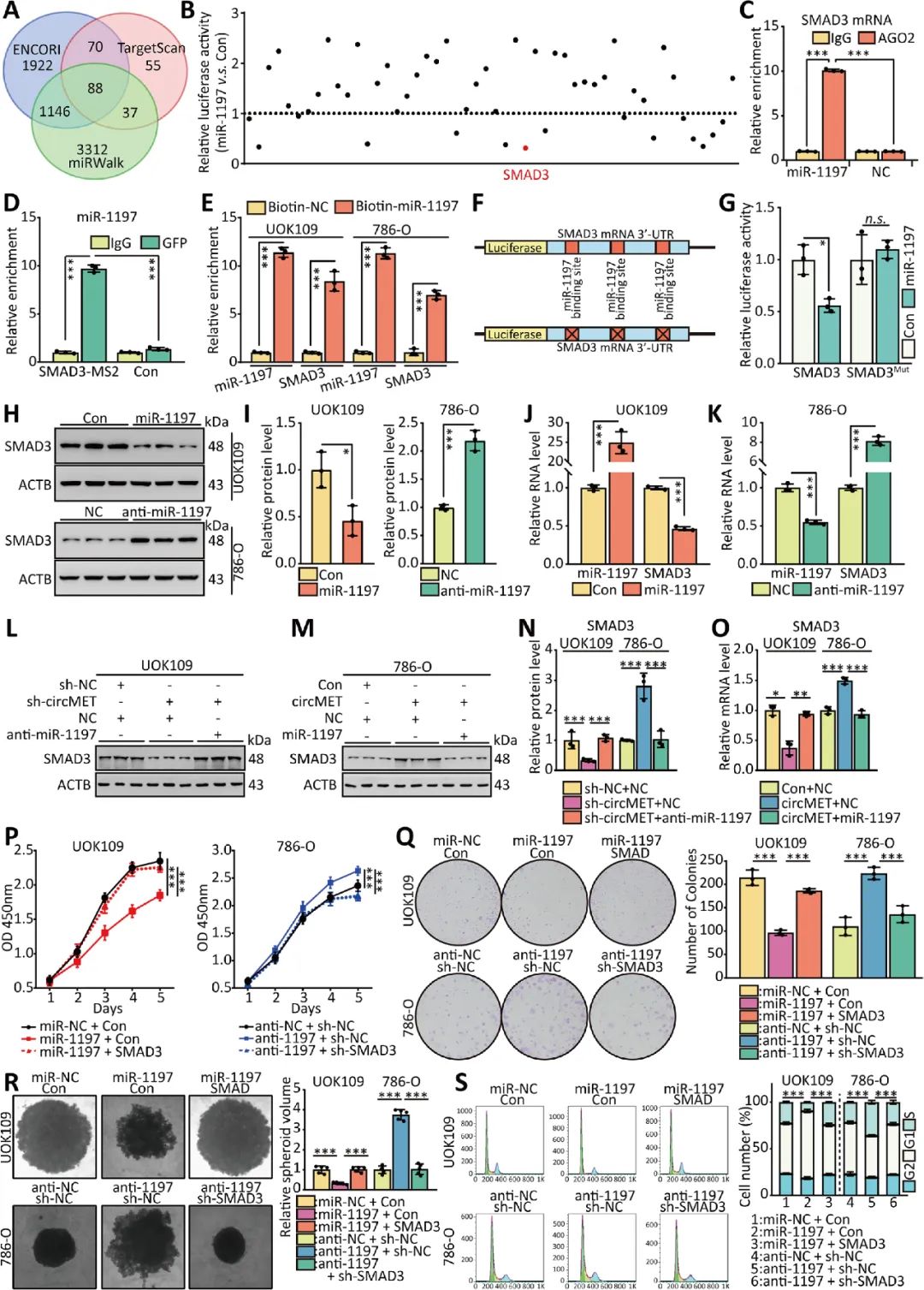 图8 CircMET经由过程转录后调控SMAD3的表达
图8 CircMET经由过程转录后调控SMAD3的表达本文研究发明NONO-TFE3交融可上调NONO-TFE3 tRCC构造以及细胞中circMET的表达,过表达circMET可显著促成NONO-TFE3 tRCC的生长。YTHDC1经由过程与m6A润色联合,促成circMET的胞质输出。circMET不只可以经由过程充任miRNAs的 吸附剂 调控SMAD3的表达,还可以经由过程间接与mRNA联合调控CDKN2A mRNA的不变性(图9)。CircMET有可能成为NONO-TFE3 tRCC和其他高表达CircMET的癌症份子医治的新靶点。
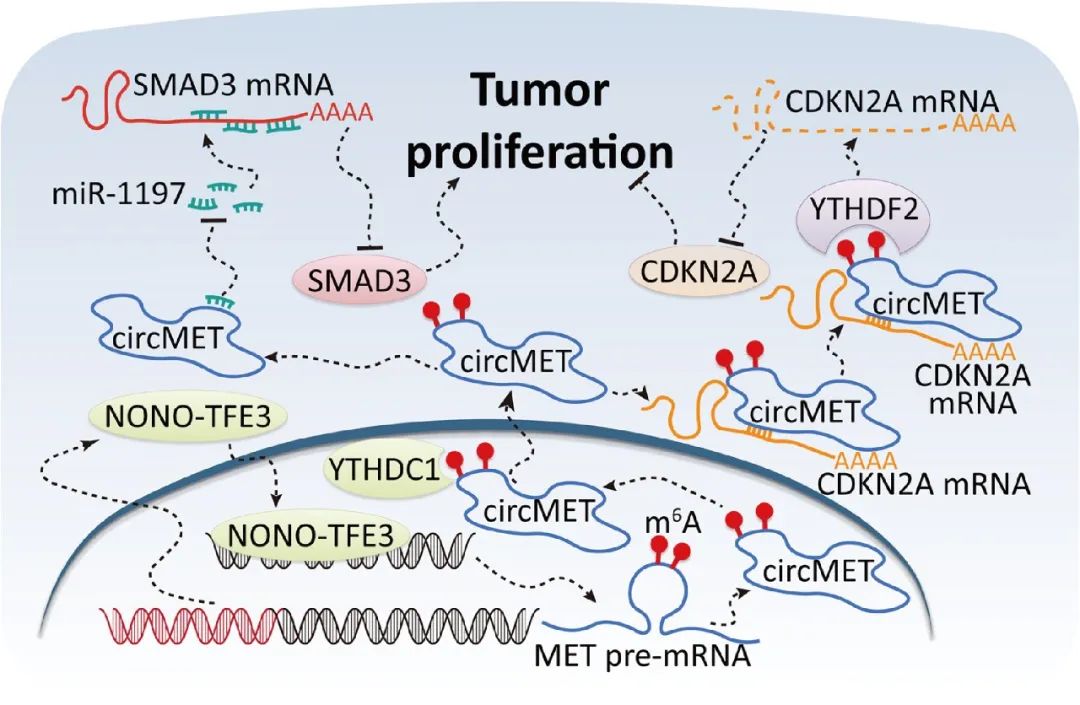
以及元生物有幸为本研究提供慢病毒载体构建以及病毒包装办事,用现实步履助力肿瘤研究!
参考文献: Moch H, Cubilla AL, Humphrey PA, Reuter VE, Ulbright TM. The 2016 WHO Classification of Tumours of the Urinary System and Male Genital Organs Part A: Renal, Penile, and Testicular Tumours. Eur Urol. 2016;70:93 105. Goodall GJ, Wickramasinghe VO. RNA in cancer. Nat Rev Cancer.2021;21:22 36 Chen L, Shan G. CircRNA in cancer: Fundamental mechanism and clinicalpotential. Cancer Lett. 2021;505:49 57. Lei Yang, Yi Chen., et al. CircMET promotes tumor proliferation by enhancing CDKN2A mRNA decay and upregulating SMAD3. Mol Cancer.2022 Jan 18;21(1):23.doi: 10.1186/s12943-022-01497-w.